
英语原文共 6 页,剩余内容已隐藏,支付完成后下载完整资料
羟基磷灰石对水溶液中氟离子的吸附行为
M. Jimeacute;nez-Reyes, M. Solache-Riacute;os
Instituto Nacional de Investigaciones Nucleares, Depto. de Quiacute;mica, Apdo. Postal 18-1027, 11801 Meacute;xico, D.F., Mexico
摘要:本文研究了pH,接触时间,氟离子浓度和吸附剂用量对羟基磷灰石吸附氟离子的影响。 在16小时的接触时间内达到平衡,氟离子的最大吸附的pHeq范围在5和7.3之间。通过使用0.01 g羟基磷灰石和25 mL溶液测定吸附系统的最高效率。伪二级模型描述了动力学吸附过程,而Freundlich模型描述了吸附等温过程。这些结果表明在该合成材料上的吸附行为是化学吸附。同时,本文也研究了使用碱性溶液解吸部分氟离子。
关键词:氟离子;吸附;羟基磷灰石
- 引言
氟离子是人类和动物的必需成分,但摄入的总量或其在饮用水中的浓度必须在一定限度内[1]。例如,根据世界卫生组织(WHO)标准规定,氟离子的允许限量为1.5 mg·Lminus;1。与氟相关的健康威胁是世界上许多地区的主要环境问题。当氟化物浓度高于允许限度时,会引起牙齿和骨骼氟中毒,骨病,牙齿斑点和甲状腺,肝脏和其他器官的损伤[2]。地下水或地表水的氟污染可能来自天然地质或使用含氟化合物作为原料的工业生产[3]。
用于除去氟离子的常规方法是用钙的化合物沉淀。然而,由于产物的溶解度较高,它们不能将氟离子降低到WHO要求的水平[4]。还有几种方法,如吸附,离子交换,电解和沉淀,已被用于除氟[3]。诸如磷酸钙、骨炭、磷灰石、活性氧化铝、活性炭等材料已被试验用于以去除氟化物。最近,水滑石类化合物及其煅烧材料已被用于相同的目的[3,5-7]。Sundaram等人[15]在固定条件下,对羟基磷灰石作为吸附剂进行了研究[8]或考虑了一些重要参数的影响,如接触时间[9-12]、吸附剂剂量[9-11]、粒径[10]、溶液pH [9-11,13]、其他阴离子[9]和氟离子浓度[9-11,13,14]的存在。考虑了接触时间、pH值、其他阴离子的影响,以及氟离子在纳米羟基磷灰石或几丁质复合物中的吸附浓度。本文的目的是通过不同的方法对pH、接触时间、氟离子浓度和吸附剂剂量等参数进行系统研究,以阐明羟基磷灰石对氟离子的吸附行为以及脱附行为。
- 材料和方法
2.1吸附剂和溶液
羟基磷灰石根据其他地方报道的技术制备[8]。 将该羟基磷灰石研磨并过筛,选择直径
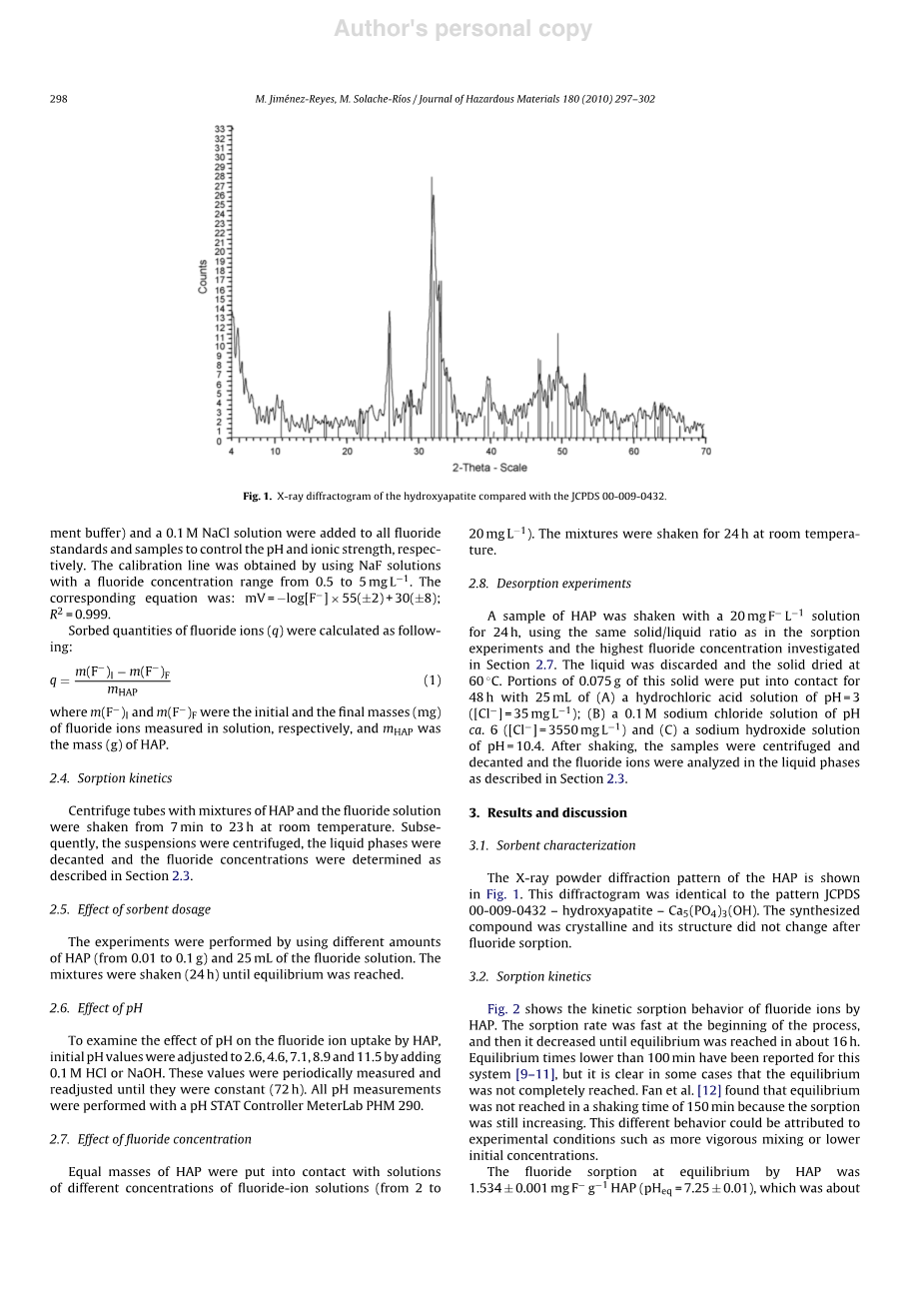
图1 与JCPDS 00-009-0432相比,羟基磷灰石的X射线衍射图
20至30目之间的颗粒用于实验。
对于本研究,除了在吸附剂剂量变化的实验中,均采用批量处理系统,其中25 mL的氟化钠溶液(Fminus;浓度为5 mg·Lminus;1)和0.075 g的HAP。每个实验进行两次。
2.2 X-ray diffraction (XRD)
使用耦合到铜-阳极X射线管的Siemens D500衍射仪获得羟基磷灰石的粉末衍射图。 常规衍射图用于鉴定化合物并验证其晶体结构。
2.3氟离子的测定
溶液中氟离子的浓度由氟离子选择电极(ISEC301F氟化物电极)测定。将TISAB II(总离子强度调节缓冲液)和0.1 M的NaCl溶液分别加入到所有氟化物标准品和样品中以控制pH和离子浓度。通过使用氟离子浓度范围为0.5至5 mg/L的NaF溶液获得标准线。相应的等式为:mV = -log [Fminus;]times;55(plusmn;2) 30(plusmn;8); R2 = 0.999。
氟离子吸附量(q)的计算公式如下:
(1)
其中和分别是在溶液中测量的氟离子的初始质量和最终质量(mg),是HAP的质量(g)。
2.4吸附动力学
将具有HAP和氟化物溶液的混合物的离心管在室温下振荡7分钟至23小时。 随后,将悬浮液离心,倾析出液相,并如2.3所述测定氟化物浓度。
2.5吸附剂用量的影响
通过使用不同量的HAP(0.01至0.1 g)和25 mL氟化物溶液进行实验。振荡混合物(24小时)直至达到平衡。
2.6 pH的影响
为了检验pH对HAP吸收氟离子的影响,通过加入0.1 M的HCl或NaOH将初始pH值调节至2.6、4.6、7.1、8.9和11.5。 定期测量并重新调整这些值,直到它们恒定(72小时)。使用pH STAT Controller MeterLab PHM 290测量所有的pH。
2.7氟离子浓度的影响
将等质量的HAP与不同浓度的氟离子溶液(2至20 mg·Lminus;1)的溶液接触。在室温下,将混合物振荡24小时。
2.8解吸实验
使用与吸附实验中相同的固液比和2.7中研究的最高氟离子浓度,将HAP样品与20 mg·Lminus;1的Fminus;溶液一起振荡24小时。滤去液体,固体在60℃下干燥。将0.075 g该固体的部分与25 mL(A) pH = 3的盐酸溶液([Clminus;] = 35 mg·Lminus;1)接触48小时;(B)pH=6的0.1 M氯化钠溶液([Cl minus;] = 3550 mg·Lminus;1)和(C)pH = 10.4的氢氧化钠溶液。振荡后,将样品离心并倾析,并如2.3所述在液相中分析氟离子。
- 结果和讨论
3.1吸附剂表征
HAP的X射线粉末衍射图如图1所示。该衍射图与JCPDS 00-009-0432-羟基磷灰石-Ca5(PO4)3(OH)图案相同。合成的化合物是结晶结构的,其结构在氟化物吸附后没有变化。
3.2吸附动力学
图2显示了HAP对氟离子的动力学吸附行为。在该过程开始时吸附速率很快,然后它在约16小时处降低直至达到平衡。 已有研究表明该系统的平衡时间低于100分钟[9-11],但在某些情况下很明显没有完全达到平衡。范等人[12]发现在150分钟的摇动时间内没有达到平衡,因为吸附量仍在增加。这种不同的行为可归因于实验条件,例如更剧烈的混合或更低的初始浓度。
图2 羟基磷灰石从水溶液中吸附氟离子与时间的函数(圆圈)
动力学拟二阶模型应用于羟基磷灰石从水溶液中吸附氟离子与时间的函数(三角形)
图3吸附剂用量对羟基磷灰石对水溶液氟离子吸附的影响
圆圈:吸附Fmacr;的百分比;三角形:平衡时吸附的氟离子的量(mg Fmacr;g-1 HAP)
该线的方程式如下: = -3.3 (plusmn; 0.2)times;() - 2.2(plusmn;0.2);R2= 0.996。
HAP在平衡状态下对氟化物吸附量为1.534 plusmn; 0.001 mgFminus;/g HAP(pHeq = 7.25 plusmn; 0.01),比Al-Mg、Al-Co、Al-Ni类水滑石化合物报道的值高约5倍[7]。
通过线性回归分析将数据拟合至动力学模型(Largergren、Elovich和伪二阶模型)。
3.2.1 Lagergren一级模型[16]
该模型由以下等式表示:
(2)
其中(mg·gminus;1)是在时间t(h)时HAP吸附的氟离子的量; (mg·gminus;1)是HAP在平衡时吸附的氟离子的量;(h minus;1)是Lagergren速率常数。
方程(1)的线性形式可表示为:
(3)
表1所示相关系数显示实验数据不适合该模型,计算的Largergren速率常数在表1中给出。
3.2.2 Elovich模型
Elovich速率方程已用于固体上气体的化学吸附动力学。 然而,一些研究人员已将该模型应用于固液吸附系统[17]。 该模型通过以下等式以线性形式表示:
(4)
其中(mg·gminus;1)是在时间t(h)时HAP吸附的氟离子的量; a(mg·gminus;1·hminus;1)是氟离子的吸附常数,b(g·mgminus;1)是氟离子的解吸常数。
方程和相应参数的值包括在表1中。然而,相关系数表明实验数据不适合该模型。
3.2.3 伪二阶模型[18]
模型的线性形式可以由以下方程表示
(5)
表1动力学模型应用于实验数据
|
模型 |
方程 |
参数 |
|
Lagergren一级模型a |
ln(1 minus; qt /qe ) = minus;0.48(plusmn;0.03); R2=0.94 |
Kt = 0.48 hminus;1 |
|
Elovich模型 |
qt = 0.25(plusmn;0.03) times; lnt 0.90(plusmn;0.06); R2=0.96 |
a = 7.14 mg gminus;1 hminus;1 b = 3.54 mg gminus;1 hminus;1 |
|
伪二阶模型 |
t/qt = 0.631(plusmn;0.009) times; t 0.44(plusmn;0.08); R2=0.996 |
K = 0.91 g mgminus;1 hminus;1 qe = 1.56 mg gminus;1 |
注:a qe (tge;16h)= 1.534 plusmn; 0.001 mg gminus;1
其中K(g·mgminus;1·hminus;1)是伪二阶常数; (mg·gminus;1)是在时间t(h)时HAP吸附的氟离子的量,(mg·gminus;1)是HAP在平衡时吸附的氟离子的量。
实验数据非常适合该模型。图2显示了实验结果的线性拟合,其方程和相应的参数包括在表1中。计算的值,作为伪二阶模型的参数,为1.56 mg Fminus;·gminus;1 HAP,这与实验非常相似(1.53 mg Fminus;·gminus;1 HAP)。
伪二阶模型基于以下假设:限速步骤是通过吸附剂和吸附物之间共享或交换电子而涉及化合价变化的化学吸附过程。尽管实验数据可以拟合到其他方程,但是最拟合于伪二阶模型,其通常应用于涉及化学反应的合成材料。
3.3吸附剂用量的影响
随着吸附剂用量的增加,HAP对氟离子的吸附能力从0.01增加到0.1 g。图3显示了在pHeq = 7.5 plusmn; 0.1时氟离子吸附容量与吸附剂剂量(HAP 质量/体积溶液)的关系。通过使用0.01 g羟基磷灰石(4.7 mg Fminus;·gminus;1 HAP)发现最大吸附容量。其他地方报道了相似的实验现象,但发现吸附能力较低[11],这可能是由于振荡时间短于达到吸附平衡所需的时间或由于材料的其他性质,如较低的比表面积、较高的结晶度或不同的组合。吸附与吸附剂用量不成比例。 的实验数据的最佳拟合方程式在图3的标题中给出,其中还示出了吸附
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[19064],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 饮用水微生物群:一个全面的时空研究,以监测巴黎供水系统的水质外文翻译资料
- 步进电机控制和摩擦模型对复杂机械系统精确定位的影响外文翻译资料
- 具有温湿度控制的开式阴极PEM燃料电池性能的提升外文翻译资料
- 警报定时系统对驾驶员行为的影响:调查驾驶员信任的差异以及根据警报定时对警报的响应外文翻译资料
- 门禁系统的零知识认证解决方案外文翻译资料
- 车辆废气及室外环境中悬浮微粒中有机磷的含量—-个案研究外文翻译资料
- ZigBee协议对城市风力涡轮机的无线监控: 支持应用软件和传感器模块外文翻译资料
- ZigBee系统在医疗保健中提供位置信息和传感器数据传输的方案外文翻译资料
- 基于PLC的模糊控制器在污水处理系统中的应用外文翻译资料
- 光伏并联最大功率点跟踪系统独立应用程序外文翻译资料



