
英语原文共 5 页,剩余内容已隐藏,支付完成后下载完整资料
虾类养殖污泥中的重金属迁移性的调查-两个连续提取程序的比较
Keivan Nemati ⁎, Nor Kartini Abu Bakar, Mhd Radzi Abas
马来亚大学化学系,马来西亚吉隆坡50603
|
文章 信息 |
概要 |
|
|
文章历史 |
通过对从马来西亚雪兰莪州虾类水产养殖业采集到的样品进行各种测试,研究重金属的影响。 从分析可以看出,虾类水产养殖的污泥中,相比于Zn、Cu、Cr、Cd、Pb来说Ca、Fe、Mn高度集中。从顺序提取,Cd,Mn和Pb主要以可交换/碳酸盐形式存在,易于被浸出。 Cu和Zn主要以可氧化形式提取。用该方法提取的所有金属浓度(Cd,Zn和Cu除外)残留分数较高。 BCR方法的结果与Tessier方法完全相似。通过百分比回收率比较,BCR方法优于Tessier方法。然而对于这两种方法,百分比回收率都是可接受的。对于伪金属消化,虽然Cd的浓度小于其他重金属,但作为肥料是非常有害的,因为Cd是植物叶子或果实中残留的重金属之一。对于污泥中的Ca调查,测量显示该元素在污泥大量存在,表明污泥可用于植物生长。重金属直接消化的结果表明,通过控制这种污泥中的Cd,我们可以将这种污泥用作农业肥料,但如果是用于无果植物,则更好。 @2008 Elsevier B.V. All rights reserved |
|
|
2008年11月29日接收 2008年12月5日收录 2008年12月14日可在线获得 |
||
|
关键词: 顺序提取 BCR法 重金属 虾类养殖业 迁移性 |
- 前言
通常使用连续提取技术来分离固体样品(土壤,沉积物,污泥,固体废物等)中的金属,因为它们的浸出性。使用一系列化学试剂针对性的依次提取样品的金属。结果提供了大量有用信息以获得关于自然环境中元素的起源,生物利用度,潜在迁移率和运输 [1]。以前的大多数研究仅限于确定金属的总浓度。然而,总浓度不能提供关于潜在有毒元素的生物利用度的信息,目前金属形态是获得该信息的必要途径[2-5]。科学界已经认识到确定土壤中重金属形态的重要性,而不在是简单地评估其土壤总体浓度。这种认识对于农业产生的有机废物回收或土壤清洁技术等环境影响研究尤其重要。目前,仍然还有一些分析问题尚未解决。土壤是含有有机和无机化合物,溶液和气体的复杂界面,在各种物理化学条件(Eh,pH等)下反应。这种介质下确定金属形态,即确定含有痕量化学元素的相(或相)是一项科学挑战[6]。为了评估沉积物中重金属的迁移率,已经开发了各种顺序提取程序[7-9]。这些提取方法从3个步骤[10]变化; 4步[11]; 5步[5];到6个步骤[8],采用的提取程序显示不同的结果[12]。两种最广泛应用的金属顺序提取方案是由Tessier等人提出的。 [5]并且社会参考局(BCR)[13]已被几位作者[14]修改。该方法比较了五种(可交换的,结合到碳酸盐,与Fe-Mn氧化物结合的有机物 - 硫化物和残留物)中提取金属的两种修饰方法和四种(可交换结合到碳酸盐,结合Fe - 氧化物,与有机物硫化物和残留物结合)[5,13]。火焰原子吸收光谱法(FAAS)是使用最广泛的技术,因为沉积物和污泥中的大部分金属浓度可以使用这种技术来确定[15]。一些微量金属如Fe,Cu,Mn和Zn对于活生物体是必需的,而大多数金属在一定程度上表现出毒性危害[16]。 由于海鲜是亚洲东南部主要的食品之一,所以这些地区有大量的虾类养殖业。 收获期后,养殖场会将污泥转移到其他地方,以保持池塘的水质。 本文的目的是调查马来西亚雪兰莪州的虾类养殖污泥中重金属的迁移率。
表1 .Tessier五阶段顺序提取方案
|
步骤 |
试剂 |
目标状态 |
|
1 |
MgCl2 1 mol/l pH=7 |
可交换态 |
|
2 |
NaOAc 1 mol/l, HOAc pH=5 |
碳酸盐结合态 |
|
3 |
NH2OH.HCL 0.04 mol/l In 25% HOAc |
Fe/Mn氧化物结合态 |
|
4 |
H202 8.8 mol/l, HNO3 and NH4OAc 0.8 mol/l |
有机物和硫化物结合态 |
|
5 |
HF/HNO3/HClO4 |
残留态 |
表2 .BCR三阶段连续提取方案
|
步骤 |
试剂 |
目标状态 |
|
1 |
HOAc (0.11 mol/l) |
土壤溶液,碳酸盐 |
|
2 |
NH2OH.HCl (0.1 mol/l) |
可交换的金属 |
|
3 |
H2O2 (8.8 mol/l) 然后在pH=2下加入NH4OAc (1.0 mol/l) |
有机物和硫化物结合态 |
|
4 |
HF/HNO3/HClO4 |
残留态,非硅酸盐结合态 |
2.实验
2.1. 试剂
所有试剂均为分析试剂级别,除非另有说明。 使用双去离子水(Milli-Q Millipore18.2MOmega;/ cm电阻率)进行所有稀释。 乙酸,羟基氯化铵,过氧化氢,乙酸铵,HNO3和HF均具有超纯品质(E.Merk,Fluka)。 所有塑料和玻璃器皿均通过浸泡稀HNO3(1 9)进行清洗,并在使用前用蒸馏水冲洗。 标准金属溶液(1000mg / l)购自Merk(德国达姆施塔特),或在实验室从纯金属制备。
2.2.仪器
本研究使用火焰原子吸收光谱仪(Perkin Elmer Analyst 400,WinLab 32 Software V6.5)。 所有测量在空气/乙炔火焰中进行。 使用离心机(久保田2420)分离固相和液相。 工作元件的工作参数由制造商推荐设定。 用于测定分析物的波长(nm)如下:Cd 228.80; 铬357.87; Cu 324.75; Zn 213.86; Mn 279.48和Pb 283.31。
2.3. 采样
2007年12月马来西亚雪兰莪州排出废水后,从养殖池塘底部共收集4个污泥样本。江样品装袋,标号并返回实验室,在实验室中把样品平均分出100g的子样品。取出其中的大物体(包括石头,砖块,混凝土和砂渣),将剩余的物料在低于30℃的温度下在局部排气通风下进行风干,以除去有害挥发性成分,然后通过1mm尼龙网筛筛滤 。 然后将风干的样品再次重新分配(至约20g),并且提取两个1g样品,作为每个连续提取方法的标样。
2.4. 伪金属消化
通过用王水消化测定伪总金属含量。 将含有1g补充材料和20ml酸(15ml HNO 3 5ml HF)的容器在沙浴加热器中加热。 将消化物通过Whatman滤纸过滤到100ml容量瓶中。
2.5.顺序提取
使用两个五阶段Tessier方法(表1)和BCR推荐的三阶段程序进行连续提取(表2)。
2.6。 Tessier方案
步骤1在室温下将1g污泥在pH = 7下用8ml 1mol / l MgCl 2搅拌1小时。
步骤2将来自步骤1的固体残余物用8ml 1mol / l醋酸钠/乙酸缓冲液,pH4.5在室温下搅拌15小时。
步骤3将步骤2的固体残余物在20℃,在25℃(v / v)乙酸中的0.04ml / l羟胺盐酸盐在96plusmn;5℃下在水浴中萃取5小时30分钟。
步骤4用3ml 0.02mol / l硝酸和5ml 30%(v / v)过氧化氢萃取步骤3中的残余物。将混合物加热至85plusmn;5℃,静置2小时。然后加入3ml 30%H 2 O 2的第二份,并将混合物在恒温下加热3小时。经过冷却后,加入在20%(v / v)硝酸中的5mlof 3.2mol / l乙酸铵。然后将样品稀释至20ml,连续搅拌30分钟。
步骤五在Teflon烧杯中用氢氟酸和高氯酸的混合物消化最终的固体残余物。首先用浓HClO4(2ml)和HF(10ml)的溶液消化0.2g样品并蒸发至接近干燥;随后第二次加入HClO4(1ml)和HF(10ml),再次将混合物蒸发至接近干燥。最后加入HClO4(1ml),蒸发样品直到出现白色烟雾。将残余物溶解在浓硝酸中并稀释至25ml(表1)。
每个提取步骤后,悬浮液以4000rpm离心30分钟。 将上清液倾析并置于酸洗管中。 固体残余物用8ml去离子水冲洗。 以类似的方式将漂洗水与固体分离。 对每个步骤获得的上清液和冲洗水进行金属分析。
2.6.1.BCR方案
步骤1:
把1g淤泥渣放入100ml带有塞子的离心管,加入40ml乙酸(0.11mol / l),并在22plusmn;5℃振荡提取16小时(过夜)。萃取剂的添加和开始离心之间不应该有间隔。通过以3000rpm离心20分钟将萃取剂与固体残余物分离,将上清液倾析到聚乙烯容器中并立即分析。残余物通过加入20ml蒸馏水洗涤,在终端摇床上振荡15分钟,并以3000rpm离心20分钟。将上清液倾析并弃去。
步骤2:
将40ml新制备的盐酸羟胺(0.1mol / l)加入到离心管中的步骤1的残余物中,通过手动振荡再悬浮,然后在22plusmn;5℃下机械振荡提取16小时(过夜)。萃取剂的添加和离心开始之间不应该有间隔。通过如步骤1中的离心和倾析将提取剂与固体残余物分离。如前所述,将提取物保留在聚乙烯容器中用于分析。通过加入20ml蒸馏水洗涤残余物,在终端振荡器上振荡15分钟,并以3000rpm离心20分钟。将上清液倾析并弃去。
步骤3:
将10ml过氧化氢(8.8mol / l)小心地加入到离心管中的残余物中,并在室温下消化1小时,偶尔手动摇动。 在85plusmn;2℃下继续消化1小时,偶尔在水浴中手动摇动半小时,然后将盖子除去,通过进一步加热将体积减小到小于3ml。 再加入10ml的过氧化氢。 将容器再次覆盖并加热至85plusmn;2℃,并消化1小时,偶尔手动摇动前半小时。 除去盖子并将液体体积减少至约1ml。 将50毫升乙酸铵(1.0摩尔/升)加入到冷的湿润残留物中,并在22plusmn;5℃下振荡16小时(过夜)。 通过如步骤1中的离心和倾析将提取物与固体残余物分离。
步骤4:
将残余物用HF / HNO 3 / HClO 4消化。
3.结果与讨论
3.1.伪金属消化
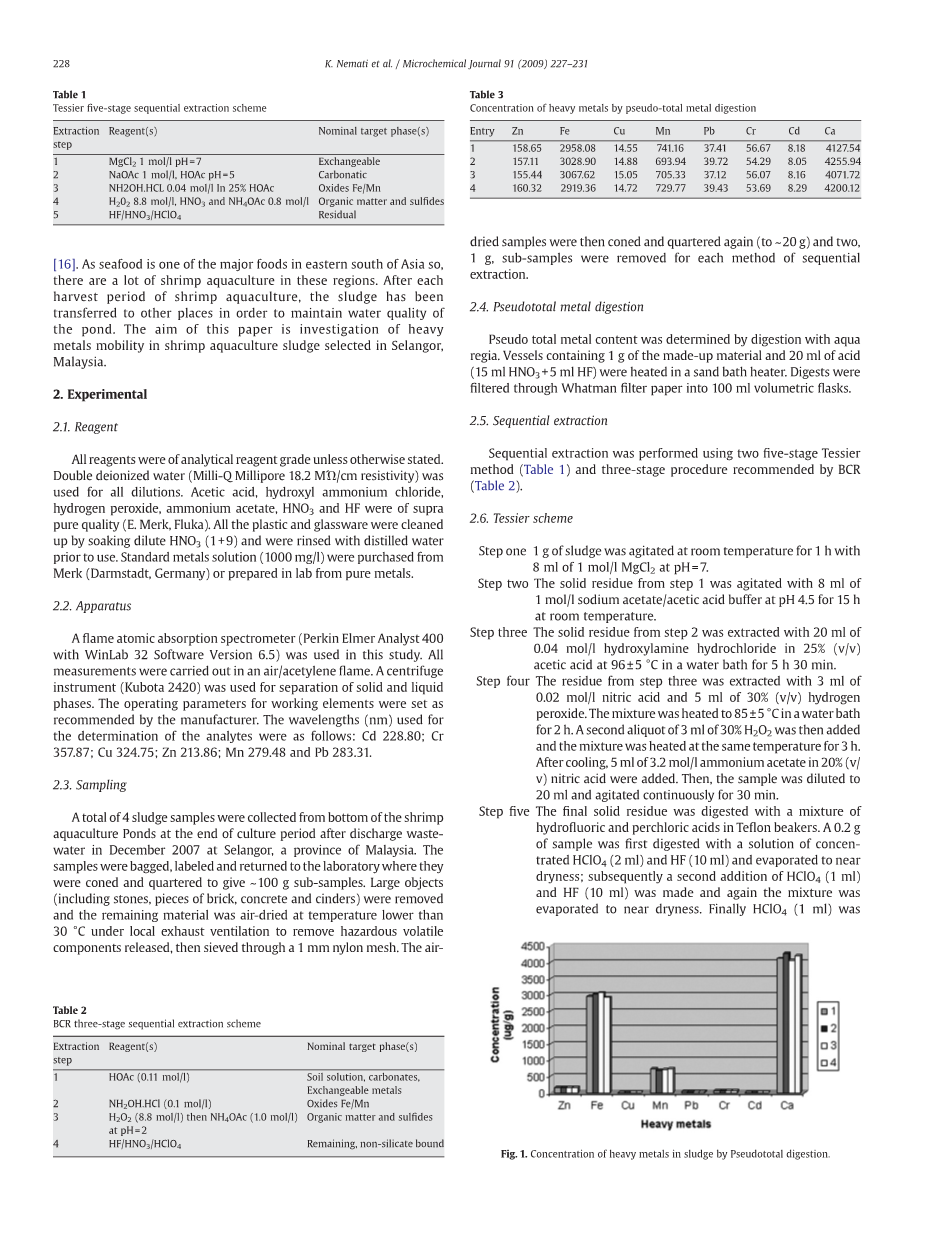
表3中给出了伪金属消解的结果,并比较了4个样品中重金属的含量。虾类养殖污泥中的主要重金属成分为Ca、Fe、Mn和Zn。与土壤重金属标准相比,本研究(除Cd)的重金属浓度均低于标准[17]。
虽然Cd的浓度小于另一种重金属,但它作为肥料是有害的,因为Cd是在植物的叶子或果实中重金属之一。重金属直接消解的结果表明,通过控制这种污泥中的Cd,我们可以将这种污泥用作农业土壤中的肥料,但最好在不结果植物中使用。
3.2.顺序提取程序
通过回收率研究检查该方法的准确性。五个阶段的回收率分别为94.42和107.59%,三阶段BCR方法在96.14和105.26%之间。本研究的结果提供了有关微量金属潜力的重要信息。结果表明,所有重金属主要与残留形态有关。
3.2.1. Tessier五步和BCR三步法
通过Tessier法和BCR法测定四种样品中重金属的浓度平均值分别见表4和表5。在该方法中,提取所有金属浓度(Cd,Zn和Cu除外)残留分数较高。在五阶段方法中可交换和碳酸盐结合的金属的比例按照以下顺序:Mngt;Fegt;Zngt;Pbgt;Crgt;Cdgt;Cu(表4和5)。
根据这些方法,在可交换态和可还原态分中发现的痕量金属的百分比非常低(镉和锰除外)。在金属研究中,Mn主要在Tessier方法的第一和第二步骤和BCR方法的第一步中提取。它代表金属与可交换和可还原相结合。另一方面,只有非常小部分的其他元素作为分数1,2分5个方法存在,分数1在BCR方法中存在。这些结果与Tuzen等人
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[26271],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 饮用水微生物群:一个全面的时空研究,以监测巴黎供水系统的水质外文翻译资料
- 步进电机控制和摩擦模型对复杂机械系统精确定位的影响外文翻译资料
- 具有温湿度控制的开式阴极PEM燃料电池性能的提升外文翻译资料
- 警报定时系统对驾驶员行为的影响:调查驾驶员信任的差异以及根据警报定时对警报的响应外文翻译资料
- 门禁系统的零知识认证解决方案外文翻译资料
- 车辆废气及室外环境中悬浮微粒中有机磷的含量—-个案研究外文翻译资料
- ZigBee协议对城市风力涡轮机的无线监控: 支持应用软件和传感器模块外文翻译资料
- ZigBee系统在医疗保健中提供位置信息和传感器数据传输的方案外文翻译资料
- 基于PLC的模糊控制器在污水处理系统中的应用外文翻译资料
- 光伏并联最大功率点跟踪系统独立应用程序外文翻译资料



